Ứng dụng cfDNA trong các xét nghiệm y khoa
ADN là vật liệu di truyền của người và phần lớn các sinh vật khác. ADN gấp cuộn nhiều cấp quanh protein histon để tạo thành cấu trúc gọi là nhiễm sắc thể. Nhiễm sắc thể tồn tại chủ yếu trong nhân tế bào, ngoài ra một lượng nhỏ ADN hiện diện trong ti thể (mtDNA). Ti thể là cơ quan của tế bào, nó có chức năng chuyển hóa đường thành năng lượng.
cfDNA hay ADN không tế bào (cell-free DNA) là những mảnh ADN được giải phóng khỏi tế bào vào hệ thống tuần hoàn của cơ thể. Loại ADN này hiện diện trong huyết tương và các chất dịch khác của cơ thể như dịch não tủy, dịch màng phổi, nước tiểu, nước bọt.
Nguồn gốc cfDNA
cfDNA huyết tương có nguồn gốc chủ yếu từ hệ thống tạo máu của những người khỏe mạnh. Tuy nhiên, các trường hợp sinh lý hoặc bệnh lý bao gồm mang thai, ghép tạng và ung thư có thể giải phóng ADN vào mạng lưới tuần hoàn ngoại vi. Do đó, xét nghiệm cfDNA trong máu có thể xác định những vấn đề sức khỏe mà không cần xâm lấn.
Các nghiên cứu đầu tiên cho rằng cái chết của tế bào (apoptosis) là nguồn gốc chính của cfDNA. Tuy nhiên, những nghiên cứu chuyên sâu hơn cho thấy cfDNA chủ yếu bắt nguồn từ apoptosis, hoại tử (necrosis) và sự bài tiết chủ động của tế bào.
cfDNA từ khối u ung thư
cfDNA từ tế bào ung thư được gọi là ADN khối u tuần hoàn (circulating tumor DNA – ctDNA). Khi một khối u hình thành và phát triển, các tế bào chết đi rồi được thay thế bằng những tế bào mới. Các tế bào chết bị phá vỡ thành nhiều thành phần bao gồm cả ADN được giải phóng vào máu. ctDNA là những đoạn ADN nhỏ với chiều dài ít hơn 200 nucleotide.
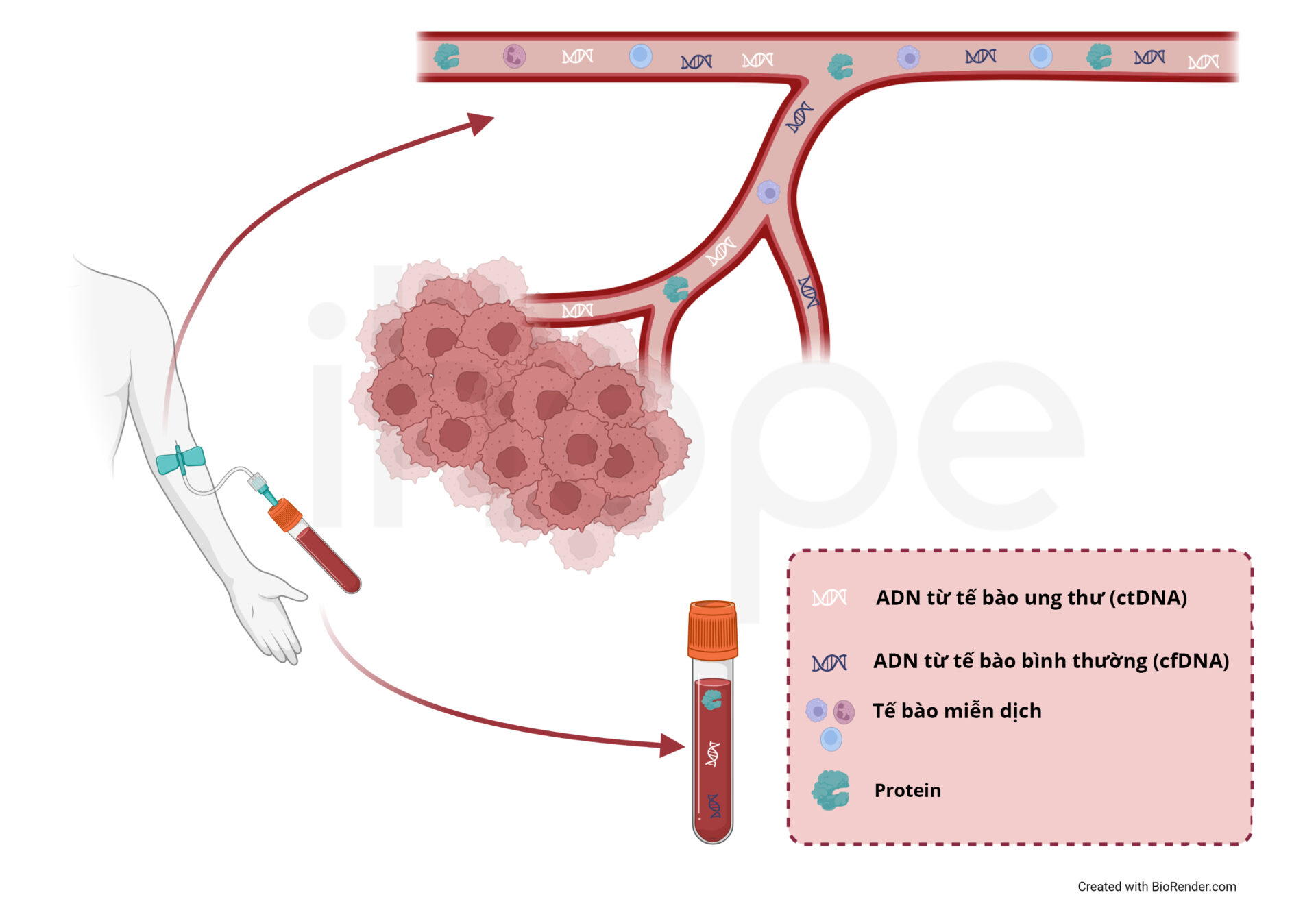
Nguồn: The National Center for Circulating Tumor DNA Guide Cancer Treatment
Lượng ctDNA khác nhau giữa các cá thể và phụ thuộc vào loại khối u, vị trí, và giai đoạn ung thư. Tế bào khối u phân chia nhanh hơn tế bào bình thường dẫn đến tỉ lệ giải phóng ctDNA cao.
cfDNA từ bào thai
Tương tự ctDNA, khi phụ nữ mang thai, một lượng cfDNA được giải phóng từ tế bào nhau thai vào máu mẹ. Những đoạn ADN này được gọi là cffDNA (cell–free fetal DNA), chúng có trình tự gen giống với ADN của thai nhi. Phân tích cffDNA có thể phát biết sớm nguy cơ cao dị tật bẩm sinh mà không cần xâm lấn.
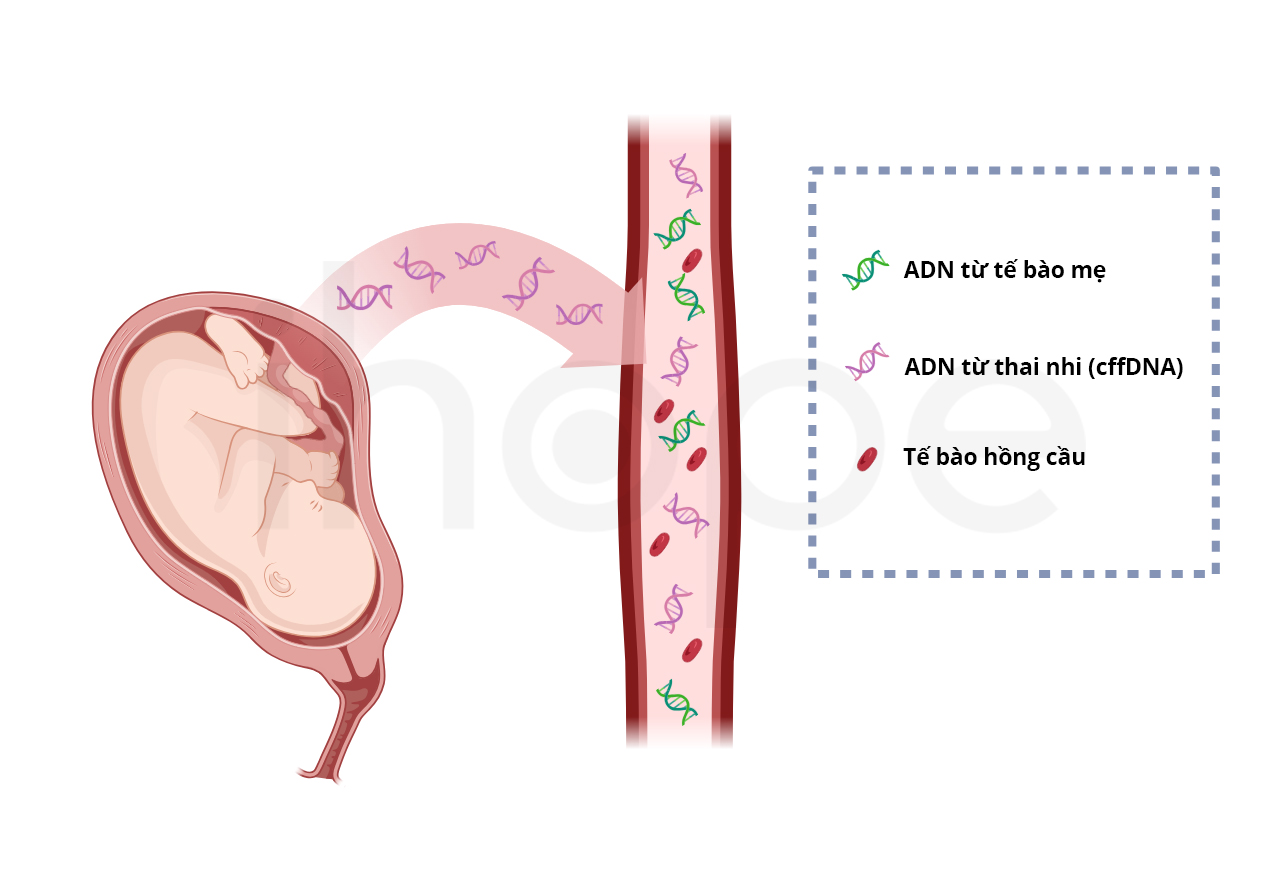
Nguồn: ihope.vn
Ứng dụng của cfDNA
cfDNA được ứng dụng trong nhiều loại xét nghiệm sàng lọc và chẩn đoán, có thể tóm tắt trong bảng sau:
| Xét nghiệm | Marker | Ý nghĩa lâm sàng | Loại mẫu |
|---|---|---|---|
| Sàng lọc dị tật thai không xâm lấn (NIPT) | ADN thai nhi (cffDNA) | Phát hiện tam bội nhiễm sắc thể 13, 18, 21 Sàng lọc các bất thường nhiễm sắc thể khác |
Huyết tương hoặc huyết thanh của mẹ |
| Cấy ghép nội tạng | ADN đặc trưng của người hiến tạng | Theo dõi hiệu quả quá trình ghép tạng | Huyết tương của người nhận ghép tạng |
| Ung thư | ADN khối u tuần hoàn (ctDNA) | Chẩn đoán, dự đoán đáp ứng điều trị của ung thư Hỗ trợ tiên lượng bệnh |
Huyết tương và huyết thanh của bệnh nhân ung thư |
| Bệnh miễn dịch | Lượng cfDNA và mức độ methyl hóa LINE-1 tăng cao | Phát hiện, đánh giá diễn biến bệnh Lupus ban đỏ Theo dõi và điều trị bệnh vảy nến, đa xơ cứng tái phát, thấp khớp tự miễn |
Huyết tương hoặc huyết thanh của bệnh nhân |
Bảng-1. Ứng dụng cfDNA trong xét nghiệm y khoa
Quy trình xét nghiệm
NIPT
Xét nghiệm NIPT được thực hiện từ tuần thứ 9 trở đi của thai kỳ. Lúc này, cffDNA được giải phóng vào trong máu mẹ đủ nhiều để tiến hành thực hiện sàng lọc. Đầu tiên, kỹ thuật viên thu máu tĩnh mạch của thai phụ vào một loại ống nghiệm chuyên biệt. Ống này chứa các hợp chất nhằm bảo quản cffDNA trong huyết tương không bị tiêu hủy. Sau đó, mẫu được tách chiết rồi phân lập cffDNA khỏi máu và được định lượng.
Định lượng cffDNA có thể thực hiện bằng hai phương pháp:
- Phương pháp thông thường: đo quang phổ huỳnh quang, PCR định lượng thời gian thực (RT-PCR)
- Phương pháp hiện đại: giải trình tự thế hệ mới (NGS), kỹ thuật digital droplet PCR (ddPCR)
Sau khi định lượng, người ta so sánh dữ liệu các đoạn cffDNA và đánh giá thể khảm. Cuối cùng, kỹ thuật viên sẽ trả kết quả.
Hiện nay xét nghiệm NIPT ihope đã có mặt tại Việt Nam với nhiều gói dịch vụ đa dạng, có thể làm sớm ngay từ tuần thứ 9 để phát hiện các bất thường nhiễm sắc thể về số lượng, cấu trúc và đột biến điểm. Công nghệ giải trình tự gen thế hệ mới NGS được ứng dụng để thực hiện xét nghiệm, kết quả cho độ chính xác cao trên 99% cho các hội chứng phổ biến như Down.
Tại các nước phát triển như Mỹ, Nhật, Hàn Quốc,… xét nghiệm NIPT được thực hiện thường quy cho tất cả thai phụ, thay thế hoàn toàn phương pháp xét nghiệm sinh hóa (Double test và Triple test) vì tính chính xác và độ tin cậy cao hơn rất nhiều.
Yêu cầu mẫu NIPT
Phân số thai nhi (fetal fraction) hay chỉ số FF là lượng ADN tự do của bào thai (cffDNA) trong tổng số cfDNA. Tỉ lệ này càng cao càng dễ dàng phân biệt giữa ADN thi và ADN của mẹ. Từ đó, kết quả xét nghiệm chính xác và đáng tin cậy hơn.
Đối với xét nghiệm NIPT, lượng cffDNA cần đạt một mức nhất định để máy có thể phân tích và cho ra kết quả. Dưới giá trị ngưỡng này, độ nhạy và đặc hiệu của kỹ thuật giảm mạnh. cffDNA tăng từ tuần thứ 6 của thai kỳ, tuy nhiên, đến tuần thứ 9 trở đi mới đạt giá trị ngưỡng để thực hiện xét nghiệm.
Một số yếu tố làm giảm lượng cffDNA trong mẫu xét nghiệm bao gồm:
- Sai quy trình lấy mẫu, bảo quản và vận chuyển
- Ống chứa mẫu không chuyên biệt
- Trình độ và kỹ thuật phòng thí nghiệm
Ngoài ra, thời điểm xét nghiệm cũng rất quan trọng, phần lớn các mẫu thu trước tuần thứ 9 thường có chỉ số FF không đủ. Ngoài ra, lượng cffDNA của các trường hợp mang thai đôi thường thấp hơn so với bình thường.
Chẩn đoán và tầm soát ung thư sớm
Tương tự NIPT, người ta cũng thu nhận ctDNA từ huyết tương của bệnh nhân. Sau đó, mẫu được thực hiện kiểm tra bằng các phương pháp như giải trình tự thế hệ mới NGS, real-time PCR, PCR kỹ thuật số hoặc đo khối phổ.
cfDNA là các đoạn ADN có mức độ phân mảnh cao, nên tổng lượng ctDNA có thể chỉ chiếm 0,01% tổng số cfDNA. Bởi vì nồng độ cực thấp này, rất khó phát hiện bệnh, đặc biệt với khối u giai đoạn đầu. Do đó, có 2 hướng để khắc phục. Phương pháp đầu tiên, một hoặc vài đột biến đặc trưng của khối u bắt nguồn từ khối u nguyên phát được nhắm mục tiêu. Người ta sẽ tập trung tìm và phát hiện các bất thường này. Phương pháp thứ 2, phân tích ctDNA nhằm giải trình tự toàn bộ bộ gen để xác định các sai khác về số lượng bản sao (CNA). Ngoài ra, người ta còn phát hiện các đột biến điểm bằng giải trình tự toàn bộ gen (Whole Genome Sequencing – WGS) hoặc giải trình tự exome (Whole Exome Sequencing – WES).
Hiện nay, xét nghiệm FoundationOne Liquid CDx ứng dụng kỹ thuật phân tích các đột biến khối u thông qua ctDNA, bệnh nhân có thể sử dụng kết quả để dùng các loại thuốc trúng đích, từ đó hiệu quả điều trị có thể được nâng cao.
Hạn chế của cfDNA
NIPT
NIPT vẫn là một xét nghiệm sàng lọc nên không dùng để chẩn đoán. Nếu kết quả NIPT cho thấy nguy cơ cao, bác sĩ sẽ chỉ định xét nghiệm chọc ối nhằm đưa ra kết quả chẩn đoán.
Sàng lọc dựa trên cfDNA chưa thể kiểm tra tất cả các bệnh di truyền. Kết quả xét nghiệm nguy cơ thấp chưa thể đảm bảo thai nhi không mang các bất thường ngoài phạm vi xét nghiệm.
Chi phí thực hiện NIPT trở thành rào cản một bộ phận dân tiếp cận với xét nghiệm. Ngoài ra, đối với các quốc gia chuộng sinh con trai, biết trước giới tính thai nhi dẫn đến tăng tỉ lệ phá thai nhằm chọn lọc giới tính.
Chẩn đoán và tầm soát ung thư
Hạn chế lớn nhất trong chẩn đoán và tầm soát ung thư thông qua cfDNA là nồng độ ctDNA quá thấp. Khi được giải phóng vào máu, cfDNA (bao gồm ctDNA từ khối u) sẽ bị enzym nuclease phân cắt thành các đoạn ngắn hơn, do đó rất khó để phân tích. Những đoạn ctDNA về bản chất vẫn là gen trong nhân tế bào, do đó, chúng có trình tự tương đồng với ADN khỏe mạnh của bệnh nhân, nên rất khó phát hiện các đặc điểm của ung thư. Ngoài ra, nhiều dấu hiệu cần được kiểm tra đồng thời nhằm tăng độ nhạy xét nghiệm.
Kết luận
cfDNA là những đoạn gen được giải phóng ra khỏi tế bào vào trong máu. cfDNA từ thai nhi được gọi là cffDNA, chúng được ứng dụng trong xét nghiệm sàng lọc dị tật thai không xâm lấn. Đối với chẩn đoán và tầm soát ung thư, người ta khảo sát ctDNA bắt nguồn từ khối u. Những kỹ thuật này giúp phát hiện bệnh mà không cần xâm lấn. Tuy nhiên, chúng vẫn còn một số nhược điểm như nồng độ cfDNA thấp, kết quả dương tính giả hoặc âm tính giả.
References
- National Library of Medicine. Cell-free DNA Testing in Routine Practice: Characterisation of a Cohort with Positive Results for Trisomies, Sex Chromosome Anomalies and Microdeletions. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7815335/
- National Library of Medicine. Circulating cell-free DNA for cancer early detection. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9133648/
- U.S National Library of Medicine. Prenatal Cell-Free DNA Screening. Retrieved November 27, 2023 from https://medlineplus.gov/lab-tests/prenatal-cell-free-dna-screening/
- U.S National Library of Medicine. What is circulating tumor DNA and how is it used to diagnose and manage cancer?. Retrieved November 27, 2023 from https://medlineplus.gov/genetics/understanding/testing/circulatingtumordna/
- National Library of Medicine. Cell-Free DNA: Hope and Potential Application in Cancer. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7938321/
- National Library of Medicine. Cell Free DNA as an Evolving Liquid Biopsy Biomarker for Initial Diagnosis and Therapeutic Nursing in Cancer- An Evolving Aspect in Medical Biotechnology. Retrieved November 27, 2023 from https://pubmed.ncbi.nlm.nih.gov/33308128/
- National Library of Medicine. Cell-Free Fetal Deoxyribonucleic Acid (cffDNA) Analysis as a Remarkable Method of Non-Invasive Prenatal Screening. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9642838/
- National Library of Medicine. Cell-Free DNA Screening: Complexities and Challenges of Clinical Implementation. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5548289/
- National Library of Medicine. Limitations and opportunities of technologies for the analysis of cell-free DNA in cancer diagnostics. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9336539/
- National Library of Medicine. Clinical Practice Guidelines for Pre-Analytical Procedures of Plasma Epidermal Growth Factor Receptor Variant Testing. Retrieved November 27, 2023 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8548242/