Xét nghiệm hóa mô miễn dịch
Hóa mô miễn dịch là gì?
Hóa mô miễn dịch (immunohistochemistry – IHC) là kỹ thuật quan trọng trong phòng thí nghiệm giúp bác sĩ phát hiện các dấu hiệu bệnh trong mẫu mô. Phương pháp này cho phép quan sát rõ phân bố và số lượng của một phân tử cụ thể trong mô bệnh nhân. Cơ chế chính dựa trên phản ứng kháng nguyên-kháng thể.
Hóa mô miễn dịch là một phần trong chẩn đoán bệnh, đặc biệt ung thư với nhiều ưu điểm như không cần phá hủy cấu trúc mô. Qua đó, kỹ thuật viên có thể đánh giá mô hình biểu hiện các phân tử trong môi trường vi mô.
Mục đích hóa mô miễn dịch
Hóa mô miễn dịch được thực hiện để:
- Chẩn đoán bệnh: phương pháp này cho phép bác sĩ chẩn đoán các bất thường như ung thư (ung thư biểu mô, khối u ác tính hoặc sarcoma). Ngoài ra, hóa mô miễn dịch cũng có thể xác định được nguồn gốc của ung thư di căn.
- Tiên lượng bệnh: hóa mô miễn dịch hỗ trợ xác định mức độ nguy cơ, độ nguy hiểm, giai đoạn và phân loại của ung thư. Từ đó, bác sĩ có thể đưa ra phác đồ điều trị phù hợp nhất.
- Dự đoán đáp ứng điều trị: hóa mô miễn dịch khảo sát các đặc điểm của khối u nhằm cung cấp thông tin về cách thức đáp ứng điều trị ung thư. Ví dụ, bác sĩ nhận thấy được ung thư vú và ung thư tuyến tiền liệt có khả năng phát triển khi có sự hiện diện của một số hormone (estrogen hoặc testosterone). Từ đó, liệu pháp hormone được ứng dụng trong điều trị các loại ung thư này.
- Theo dõi quá trình điều trị: bác sĩ sử dụng phương pháp này để khảo sát hiệu quả điều trị ung thư của các phác đồ được sử dụng.
Quy trình hóa mô miễn dịch
Nguyên tắc chung: hóa mô miễn dịch dựa trên liên kết kháng nguyên-kháng thể. Kháng nguyên đặc trưng của ung thư hiện diện trên bề mặt tế bào khối u. Do đó, nó trở thành dấu hiệu nhận biết bệnh. Khi thực hiện hóa mô miễn dịch, nếu khối u có kháng nguyên đặc trưng, nó sẽ liên kết với kháng thể (tương tác ổ khóa và chìa khóa) và phát ra tín hiệu huỳnh quang giúp kỹ thuật viên nhận biết.
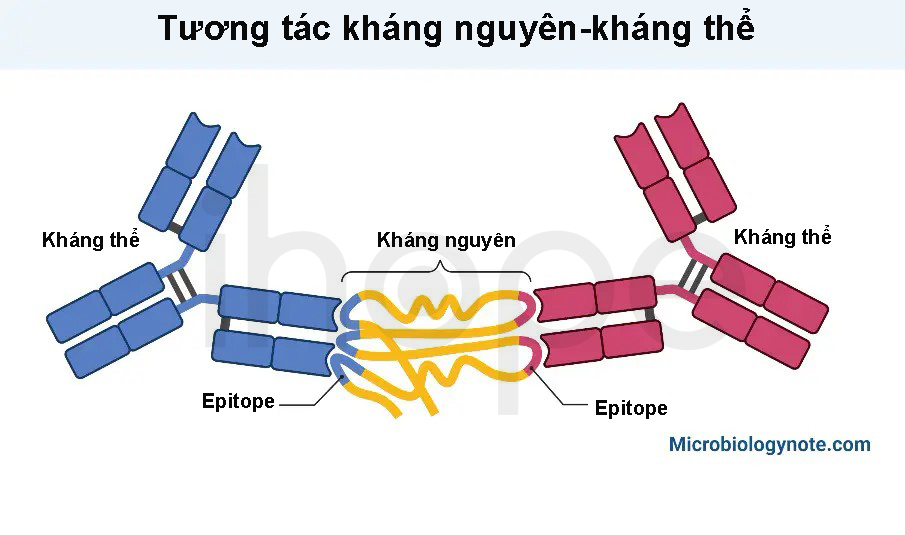
Nguồn: microbiologynote
Xử lý và cố định mô (chuẩn bị mẫu)
Cố định mẫu
Mẫu mô sau khi sinh thiết hoặc phẫu thuật cắt bỏ sẽ xảy ra hiện tượng thiếu máu cục bộ vì không được cung cấp máu nuôi. Do đó, các ADN, ARN và protein trong mẫu bị suy thoái hoặc bắt đầu phân hủy. Đồng thời, tế bào cũng chết dần theo thời gian.
Mẫu sau khi thu nhận cần được cố định trong formalin đệm trung tính 10% nhằm ngăn chặn quá trình phân hủy protein, vật chất di truyền cũng như hình thái của tế bào mô.
Phục hồi các kháng nguyên (hoặc epitope)
Quá trình cố định mô trong formalin có thể khiến các kháng nguyên trên bề mặt tế bào bị “che lấp”, nên khả năng liên kết với kháng thể suy giảm dẫn đến sai lệch kết quả. Do đó, mẫu cần trải qua bước khôi phục các kháng nguyên. Kháng thể nhận biết kháng nguyên thông qua một vùng cụ thể được gọi là epitope. Các epitope được xây dựng lại trong bước này. Từ đó, phản ứng trở nên nhạy và chính xác hơn.
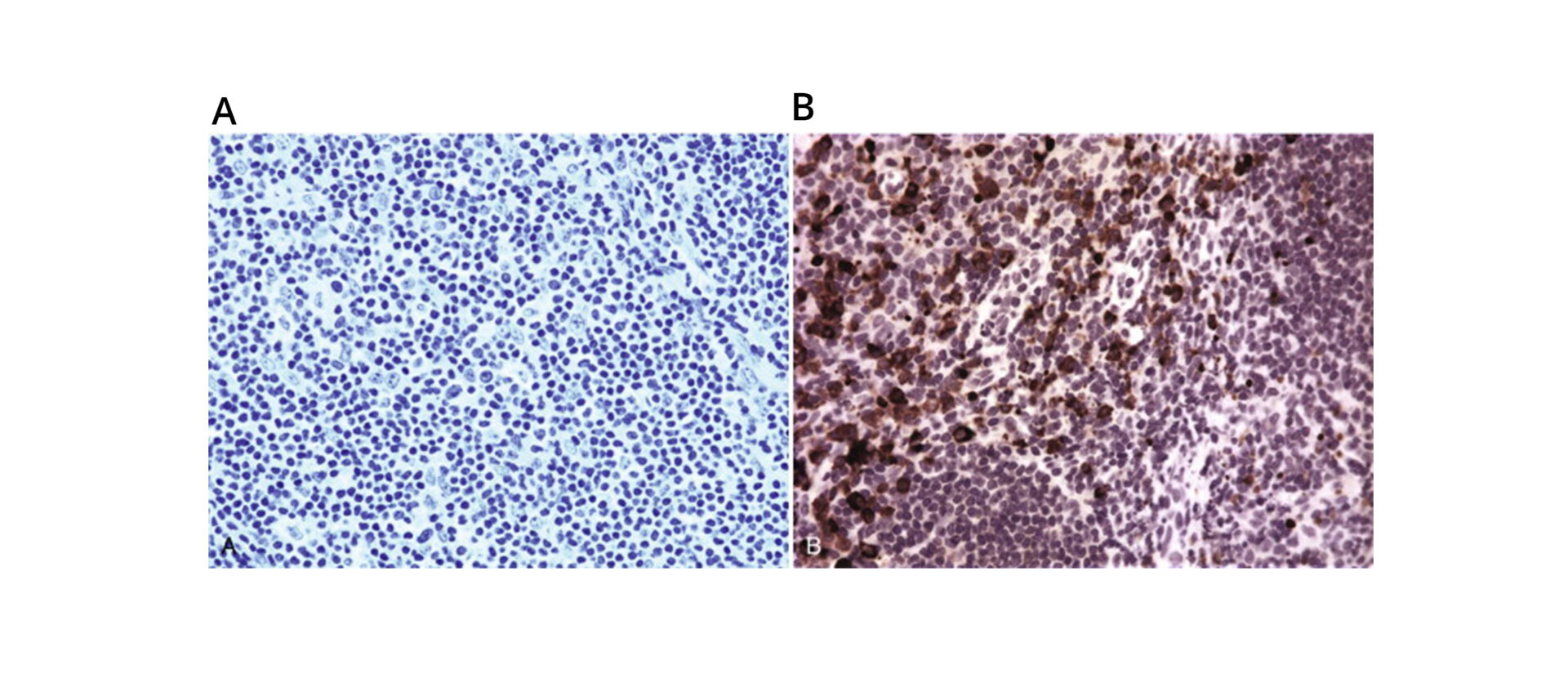
Ghi chú: (A) không có tế bào dương tính khi không khôi phục kháng nguyên, (B) các tế bào dương tính màu nâu đậm rải rác sau khi khôi phục kháng nguyên
Nguồn: Immunohistochemistry – National Library of Medicine
Phương pháp khôi phục kháng nguyên tùy thuộc vào loại mô, kháng nguyên cụ thể và cách thức bảo quản mẫu. Mục đích chính là phá vỡ các liên kết chéo của protein do bước cố định gây ra.
Hai phương pháp chính để phục hồi kháng nguyên có thể được sử dụng bao gồm:
- Xử lý vật lý: bao gồm nhiệt và sóng siêu âm
- Xử lý hóa học: sử dụng các enzyme phân hủy, chất biến tính
Trong một số trường hợp, người ta kết hợp cả hai phương pháp vật lý và hóa học. Hiện nay, phổ biến nhất là phục hồi kháng nguyên cảm ứng nhiệt (Heat Induced Antigen Retrieval – HIAR). HIAR được sử dụng bằng lò vi sóng, tấm gia nhiệt, nồi áp suất hoặc nồi hấp chuyên dụng cùng với một số điều kiện khác như pH, thời gian.
“Khóa” protein (protein blocking)
Trong mẫu mô, một số protein hoặc các cấu trúc tương tự kháng nguyên đích có khả năng liên kết với kháng thể, do đó kết quả có thể bị nhiễu hoặc khó quan sát do hiện tượng nhuộm nền (nền cũng bắt chất tạo màu). Vì vậy, khóa các protein này làm tăng độ nhận diện kháng nguyên của kháng thể.
Bất hoạt enzyme nội sinh
Peroxidase là enzyme xúc tác các phản ứng oxi hóa trong cơ thể, chúng cần phải được ngăn chặn nhằm đảm bảo các thành phần protein và chất hóa học trong mẫu được ổn định. Những mô có hàm lượng máu cao (ví dụ tại vị trí xuất huyết nặng) hoặc thâm nhiễm viêm bạch cầu hạt nghiêm trọng cần ức chế mạnh enzyme nội sinh. Hydro peroxide 3% được sử dụng phổ biến để bất hoạt peroxidase nội sinh. Tuy nhiên, một số kháng nguyên (chẳng hạn như CD4) có thể bị phân hủy bởi hydro peroxide 3%. Do đó, nồng độ thích hợp khoảng 0,5%.
Lựa chọn kháng thể
Kỹ thuật viên tiến hành đánh giá và lựa chọn các kháng thể phù hợp với mẫu mô. Điều này rất quan trọng, nó quyết định tính chính xác và độ tin cậy của kết quả. Lựa chọn kháng thể thường bắt đầu bằng cách đánh giá các loại kháng thể đã được nghiên cứu.
Kháng thể được chia thành 2 loại bao gồm:
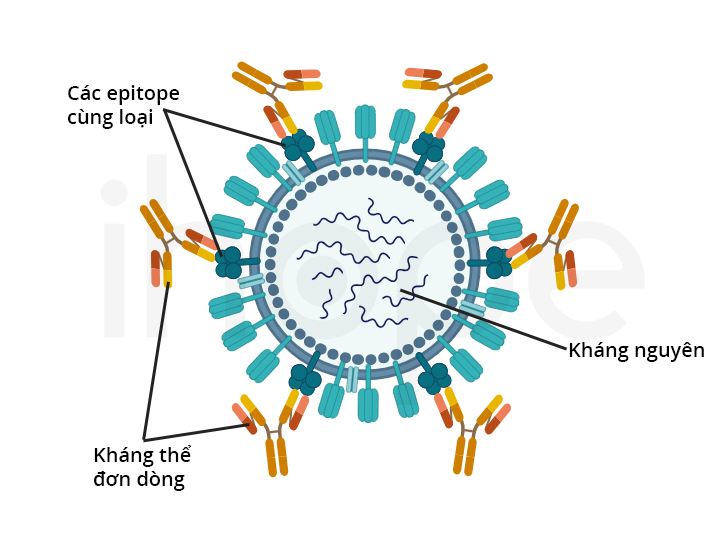
- Kháng thể đa dòng: là hỗn hợp nhiều kháng thể khác nhau. Những kháng thể này có thể gắn vào nhiều vị trí đặc hiệu (epitope) trên cùng một kháng nguyên
- Kháng thể đơn dòng: là những bản sao giống hệt nhau của cùng một kháng thể. Kháng thể đơn dòng chỉ gắn vào một vị trí đặc hiệu (epitope) trên kháng nguyên
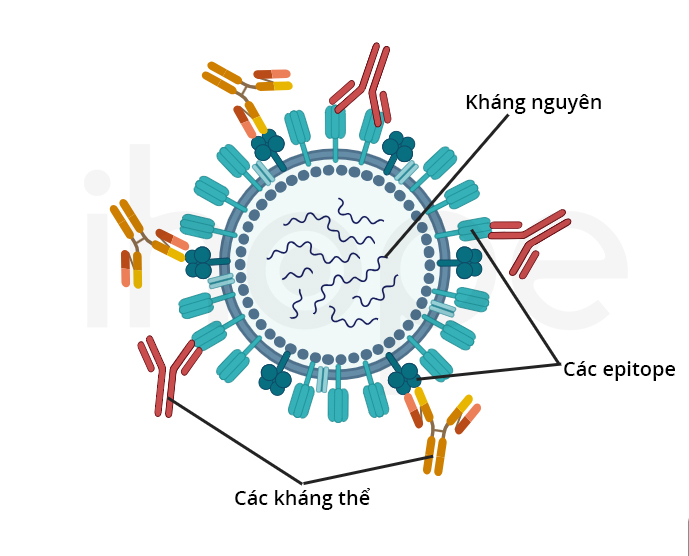
Nguồn: ihope.vn
Nguồn: ihope.vn
Để tạo ra kháng thể đa dòng, người ta sử dụng động vật thí nghiệm và kích thích kháng nguyên lặp đi lặp lại. Cụ thể hơn, con vật được tiêm kháng nguyên đã được tinh chế, sau đó cơ thể chúng tạo ra các kháng thể tương ứng. Quy trình này được lặp lại nhiều lần để thu được kháng thể từ máu hoặc huyết thanh. Do tính phức tạp và thực hiện trên cơ thể sống, khả năng tái sản xuất thấp.
Ưu và nhược điểm của kháng thể đa dòng và đơn dòng:
| Kháng thể | Ưu điểm | Nhược điểm |
|---|---|---|
| Đơn dòng | Độ đặc hiệu với epitope cao và với nền thấp | Ít nhạy đối với các epitope bị che khuất do mẫu nhúng paraffin cố định bằng formalin |
| Đa dòng | Độ nhạy cao hơn (nhận diện nhiều epitope) | Sản xuất hạn chế và khó tái sản xuất Khả năng bắt nền cao do kháng thể tự nhiên |
Bảng-1. So sánh kháng thể đơn dòng và đa dòng
Phát hiện kháng nguyên
Phát hiện kháng nguyên hay nhuộm miễn dịch là bước nhận diện sự tương tác giữa kháng nguyên và kháng thể. Có hai phương pháp chính bao gồm:
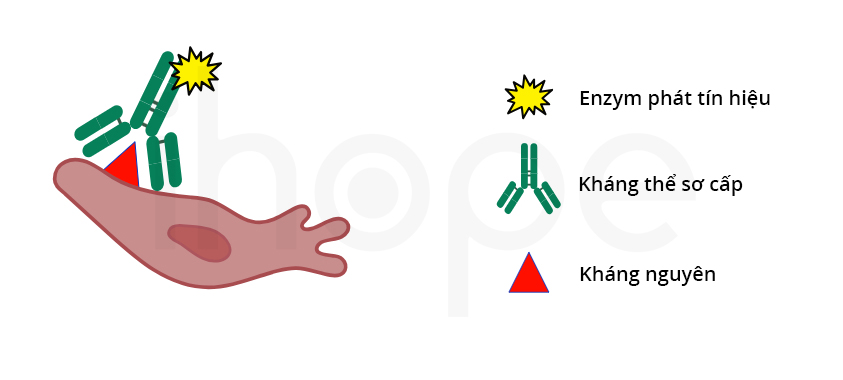
- Phương pháp trực tiếp: một kháng thể có gắn enzyme phát tín hiệu liên kết đặc hiệu với kháng nguyên. Phương pháp này được dùng chủ yếu cho các mẫu mô có mức độ biểu hiện kháng nguyên cao.
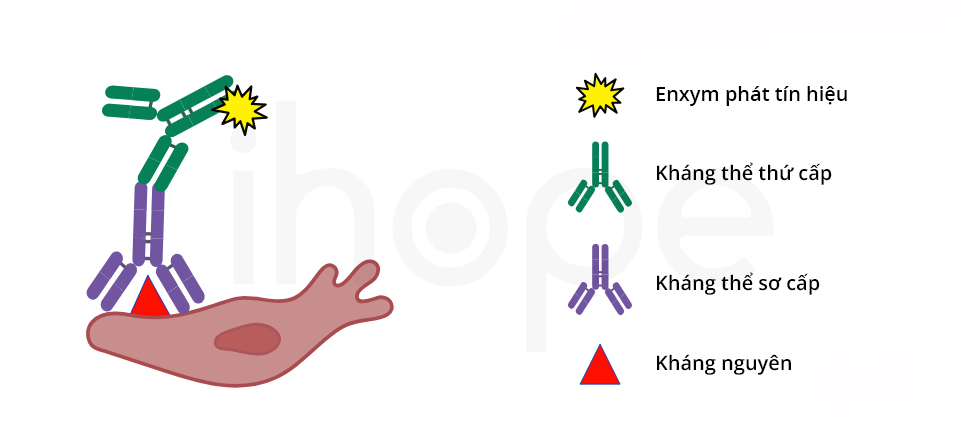
- Phương pháp gián tiếp: kháng thể sơ cấp (primary antibody) liên kết đặc hiệu với kháng nguyên của mẫu. Sau đó, các kháng thể thứ cấp (secondary antibody) có gắn các enzyme phát tín hiệu được bổ sung và liên kết với kháng thể sơ cấp.
Nguồn: ihope.vn
Nguồn: ihope.vn
Phát hiện gián tiếp được sử dụng phổ biến do làm tăng độ nhạy đối với các kháng nguyên biểu hiện thấp. Những hệ thống thường được sử dụng như phức hợp avidinbiotin, đánh dấu streptavidin biotin, phosphatase anti-phosphatase, hệ thống polymer–based, và khuếch đại tyramine.
So với các phương pháp hóa mô miễn dịch tiêu chuẩn, hệ thống phát hiện polymer-based có độ nhạy cao hơn khoảng 50 lần. Hệ thống này sử dụng polyme tổng hợp hoặc tự nhiên kết hợp đồng thời với kháng thể thứ cấp và HPR nhằm tăng khả năng liên kết với các phân tử tín hiệu của kháng nguyên.
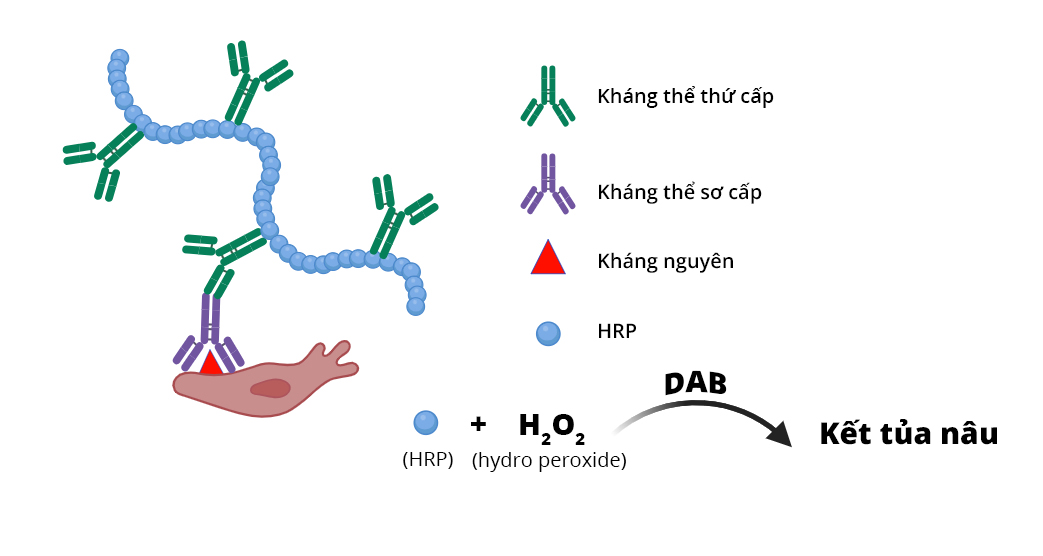
Nguồn: ihope.vn
HRP (horseradish peroxidase) là enzyme được chiết xuất từ rễ cây cải ngựa. HRP tạo phức với hydro peroxide sinh ra nước và oxy. Oxy tự do sẽ oxy hóa cơ chất là diaminobenzidine (DAB) để tạo kết tủa lắng đọng trong mô có màu nâu.
Kết quả cuối cùng được quan sát dưới kính hiển vi. Kĩ thuật viên sẽ phân tích kết quả thu được.
Hạn chế của hóa mô miễn dịch
Hóa mô miễn dịch không có tiêu chuẩn chung cho từng bước. Do đó, quy trình thực hiện được thiết kế và tối ưu hóa theo quy chuẩn của mỗi phòng xét nghiệm dẫn đến kết quả sai khác.
Kết quả xét nghiệm có thể bị dương tính giả (phát hiện một kháng nguyên không hiện diện trong mẫu mô) hoặc âm tính giả (không phát hiện được kháng nguyên hiện diện trong mô).
Một số yếu tố gây nhiễu kết quả bao gồm:
Tính sẵn có của các kháng thể
Sự ra đời và hoàn thiện kỹ thuật tế bào hybridoma có thể tạo ra số lượng lớn các kháng thể đơn dòng. Tuy nhiên, theo thời gian người ta nhận thấy các kháng thể này có tính đặc hiệu không cao như kì vọng. Nguyên nhân do các kháng nguyên phân bố rất rộng dẫn đến các kháng thể sản xuất được không bao phủ hết.
Mất tính kháng nguyên trong mẫu
Người ta cho rằng các mẫu mô được bảo quản bằng parafin và cố định trong formalin gây mất đặc tính của kháng nguyên. Mức độ có thể tùy thuộc vào thời gian bảo quản mẫu. Do đó bước phục hồi kháng nguyên được lựa chọn và thực hiện nghiêm ngặt.
Kinh nghiệm
Hóa mô miễn dịch là kĩ thuật mang tính khách quan hơn so với kiểm tra hình thái tế bào thông thường. Tuy nhiên, kinh nghiệm đánh giá các tiêu bản của kỹ thuật viên là rất quan trọng. Ngoài ra, lựa chọn phương pháp hồi nguyên kháng nguyên, loại kháng thể phù hợp và hệ thống phát hiện kháng nguyên cũng cần kinh nghiệm vững chắc.
Khi có kết quả hóa mô miễn dịch, để đánh giá chính xác, kĩ thuật viên cần nắm rõ những hạn chế của kháng thể về mặt kỹ thuật, độ đặc hiệu và độ nhạy của chúng.
Kết luận
Hóa mô miễn dịch đã trở thành công cụ đắc lực trong chẩn đoán và nghiên cứu mô bệnh học. Phương pháp này có thể nhận diện các dấu ấn sinh học đặc trưng của bệnh, qua đó một số loại thuốc có thể được cá nhân hóa. Đa phần quy trình hóa mô miễn dịch đã được tự động và tiêu chuẩn hóa, tuy nhiên còn nhiều yếu tố cần được nghiên cứu và tối ưu nhằm nâng cao độ đặc hiệu, độ nhạy và tính chính xác của xét nghiệm.
References
- Cleveland Clinic. Immunohistochemistry. Retrieved January 29, 2024 from https://my.clevelandclinic.org/health/diagnostics/25090-immunohistochemistry
- National Library of Medicine. Immunohistochemistry for Pathologists: Protocols, Pitfalls, and Tips. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5122731/
- National Library of Medicine. Immunohistochemistry for Pathologists: Protocols, Pitfalls, and Tips. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5122731/
- National Library of Medicine. An Introduction to the Performance of Immunohistochemistry. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6749998/
- National Library of Medicine. Applications of immunohistochemistry. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3467869/
- National Library of Medicine. Immunohistochemistry. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7151845/
- National Library of Medicine. Blocking endogenous peroxidases: a cautionary note for immunohistochemistry. Retrieved January 29, 2024 from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4401301/
- ScienceDirect. Immunohistochemical Detection Methods. Retrieved January 29, 2024 from https://www.sciencedirect.com/science/article/abs/pii/B9780123864567074050
- IntechOpen. Immunohistochemistry - The Ageless Biotechnology. Retrieved January 29, 2024 from https://www.intechopen.com/chapters/64808