Bệnh bạch cầu cấp dòng tủy với chuyển vị (CBF-AML)
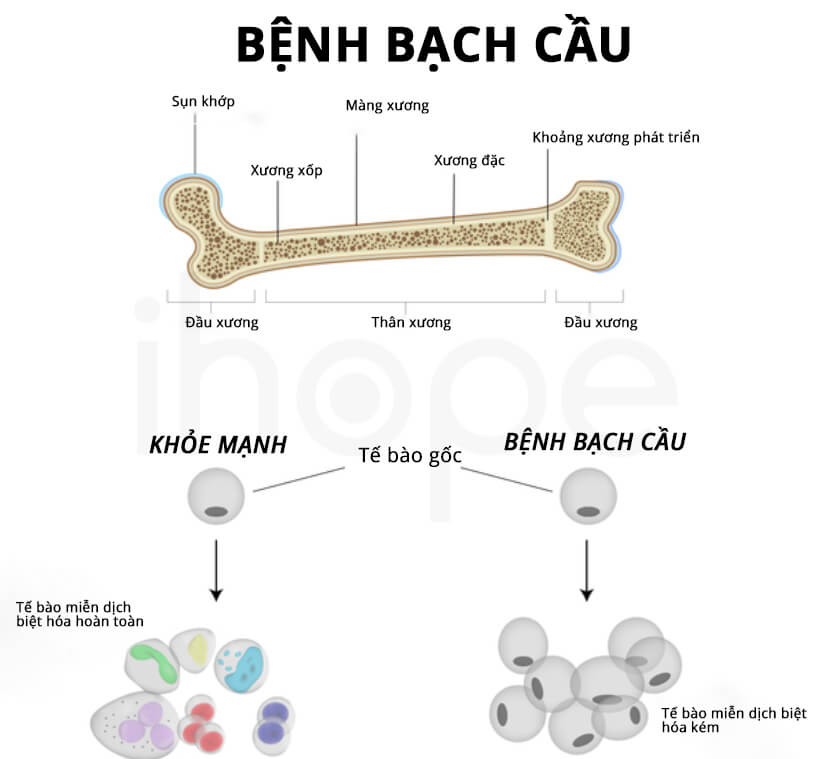
Bệnh bạch cầu cấp dòng tủy với chuyển vị (Core Binding Factor Acute Myeloid Leukemia – CBF-AML) là một dạng ung thư tủy xương. Tế bào gốc tạo máu trong tủy xương của người bình thường sẽ phát triển thành nhiều loại tế bào máu khác nhau bao gồm bạch cầu, hồng cầu và tiểu cầu. Trong khi tủy xương của bệnh nhân bạch cầu cấp dòng tủy tạo ra số lượng lớn các tế bào bạch cầu chưa trưởng thành ác tính (tế bào blast), những tế bào này tăng sinh nhanh chóng rồi di căn ra máu ngoại vi và tích lũy trong các cơ quan khác. Các tế bào bất thường không thể chống lại nhiễm trùng, chúng làm suy yếu quá trình tạo ra tế bào bạch cầu, hồng cầu và tiểu cầu có chức năng.
Nguồn: joshya/Shutterstock.com
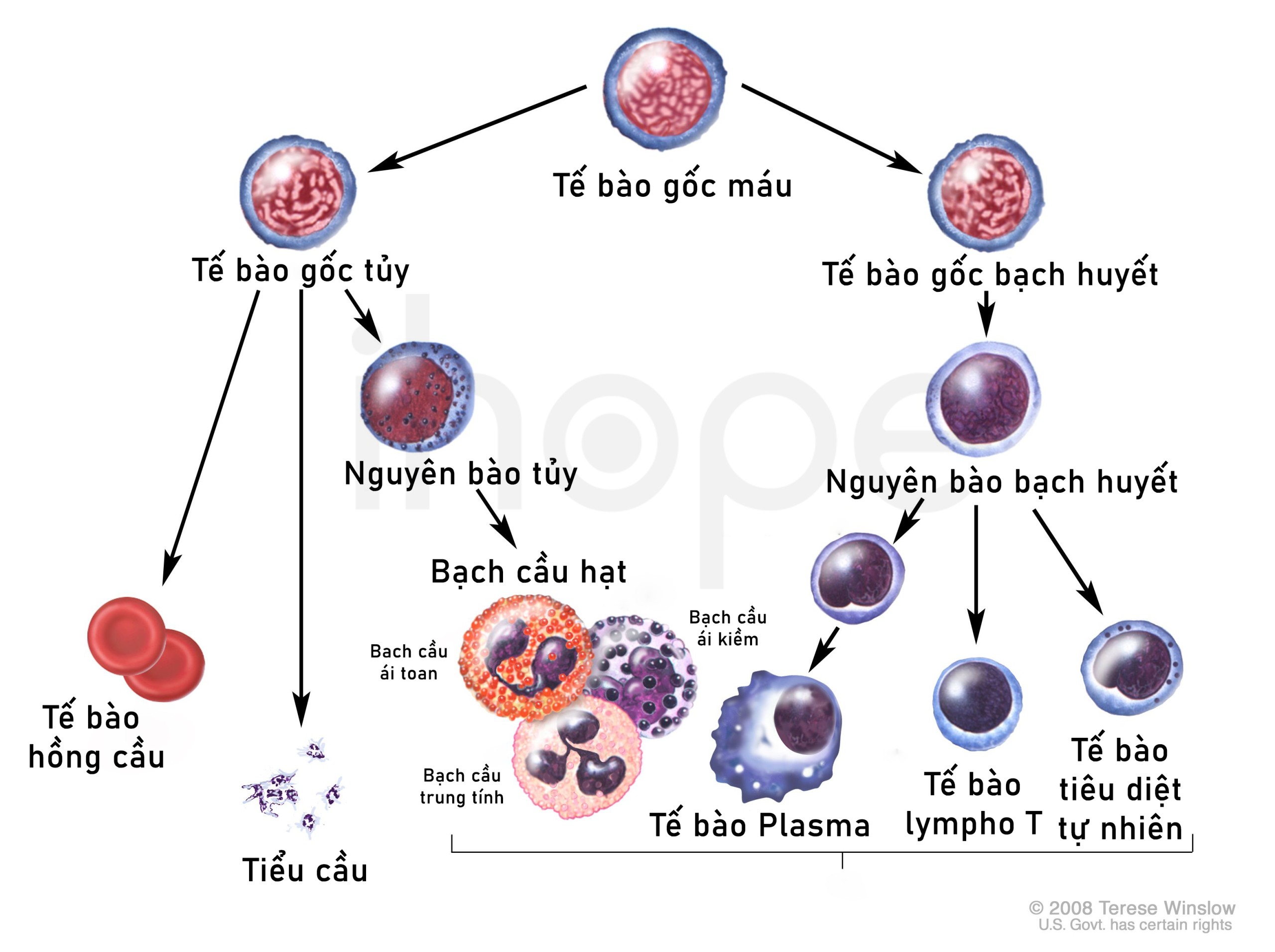
Ảnh: Quá trình phát triển của tế bào máu
Nguồn:© 2008 Terese Winslow LLC for the National Cancer Institute
Bệnh bạch cầu cấp dòng tủy với chuyển vị chiếm 12–15% trong tất cả các trường hợp mắc bệnh bạch cầu cấp dòng tủy (Acute Myeloid Leukemia – AML). Bệnh được chia thành nhiều dạng khác nhau dựa trên những biến đổi di truyền bao gồm t(8;21), inv(16) và t(16;16). Trong khi AML nói chung là bệnh của người lớn tuổi, CBF-AML thường bắt đầu trước tuổi trưởng thành và có thể xảy ra tại giai đoạn trẻ nhỏ. So với các dạng bệnh bạch cầu cấp dòng tủy khác, CBF-AML có tiên lượng tương đối tốt với khoảng 90% trường hợp khỏi bệnh sau khi điều trị. Tuy nhiên, bệnh thường tái phát sau khi điều trị thành công.
Biểu hiện lâm sàng
Người bệnh biểu hiện triệu chứng do thiếu các tế bào máu trưởng thành bao gồm:
- Dễ nhiễm trùng
- Thiếu máu
- Mệt mỏi
- Suy nhược
- Dễ bầm tím
- Chảy máu bất thường
Người bệnh có thể xuất hiện một số triệu chứng ít phổ biến hơn như sốt, khó thở, chán ăn và sụt cân.
Người ta ghi nhận một số trường hợp viêm nướu răng do bạch cầu xâm nhập vào mô nướu. Trường hợp hiếm hơn, bệnh nhân xuất hiện các khối bạch cầu cứng hoặc khối u bên ngoài tủy xương (sarcoma xương).
Độ phổ biến
Tỉ lệ mắc bệnh bạch cầu dòng tủy cấp tính khoảng 3.5/100.000 người mỗi năm. Trong đó, bạch cầu cấp dòng tủy với chuyển vị chiếm 12–15% số người bệnh trong độ tuổi trưởng thành.
Nguyên nhân
Chuyển vị giữa nhiễm sắc thể 8, nhiễm sắc thể 21 và trong nhiễm sắc thể 16 gây ra bệnh bạch cầu cấp dòng tủy với chuyển vị. Quá trình thay đổi các đoạn nhiễm sắc thể ảnh hưởng đến trình tự gen RUNX1, RUNX1T1, CBFB và MYH11.
Trong đó, gen RUNX1 và CBFB cung cấp các hướng dẫn tạo ra hai phần của phức hợp protein yếu tố phiên mã dị thể (Core Binding Factor - CBF), phức hợp này tham gia kích hoạt một số gen cần thiết cho quá trình tạo máu. Những thay đổi trong cơ chế di truyền khiến đoạn ADN từ nhiễm sắc thể 8 và 21 tách ra, sau đó chúng hoán đổi vị trí cho nhau khiến một phần gen RUNX1 trên nhiễm sắc thể 21 hợp nhất với một phần gen RUNX1T1 trên nhiễm sắc thể 8. Quá trình này được kí hiệu là t(8;21). Các gen kết hợp với nhau tạo thành một trình tự mới cung cấp thông tin tổng hợp nên protein RUNX1-ETO có khả năng gắn lên ADN mục tiêu. Tuy nhiên, thay vì kích hoạt gen mục tiêu hoạt động, protein bất thường này ức chế chúng dẫn đến các gen mục tiêu không thể biểu hiện thông tin di truyền.
Ngoài ra, những thay đổi trong gen CBFB cũng gây ra bệnh bạch cầu cấp dòng tủy với chuyển vị. Đoạn ADN trên nhiễm sắc thể 16 xảy ra đứt gãy tại 2 vị trí, sau đó chúng đảo chiều rồi gắn lại nhiễm sắc thể nhằm tạo thành một trình tự ADN mới (được kí hiệu là inv(16)). Hoạt động đảo ngược này khiến hai gen CBFB và MYH11 hợp nhất với nhau tạo ra protein CBFβ-MYH1. Ngoài ra, người ta cũng phát hiện một trường hợp chuyển vị khác liên quan đến nhiễm sắc thể 16 (được kí hiệu là t(16;16)) cũng khiến 2 gen hợp nhất nhưng trường hợp này ít phổ biến hơn. Trình tự gen mới cung cấp thông tin tổng hợp nên protein CBFβ-MYH11 có khả năng hình thành yếu tố phiên mã dị thể (CBF) nhưng chúng không có khả năng liên kết với ADN, từ đó quá trình kiểm soát hoạt động gen mục tiêu suy giảm. Ngoài ra, protein MYH11 trong yếu tố phiên mã dị thể có thể tương tác với các protein khác nhằm ngăn chặn yếu tố phiên mã dị thể hoạt động.
Những thay đổi di truyền làm cho yếu tố phiên mã dị thể thay đổi cấu trúc, nên các tế bào máu không thể trưởng thành và biệt hóa. Do đó, số lượng lớn các tế bào bạch cầu chưa trưởng thành ác tính (tế bào blast) được tạo ra. Tuy nhiên, người ta cho rằng hoạt động sắp xếp lại nhiễm sắc thể thường không đủ để gây ra bệnh bạch cầu, chúng cần thêm một hoặc nhiều thay đổi di truyền khác. Những thay đổi này có thể khiến các tế bào chưa trưởng thành phát triển và phân chia không kiểm soát, từ đó số lượng tế bào blast tăng lên quá mức để hình thành ung thư.
Chẩn đoán
Bác sĩ chẩn đoán bệnh bạch cầu cấp dòng tủy với chuyển vị dựa trên một số thông tin và xét nghiệm bao gồm:
- Phương pháp tế bào học: dựa trên phân tích tế bào theo dòng chảy nhiều thông số (multiparameter flow cytometry) nhằm xác định các dấu chuẩn sinh học trên bề mặt hoặc bên trong tế bào.
- Định lượng số tế bào blast trong tủy xương hoặc máu ngoại vi: theo ICC (International Consensus Classification), nếu một người có số lượng tế bào blast chiếm 10%, họ có nguy cơ mắc bệnh bệnh bạch cầu cấp dòng tủy với chuyển vị.
- Lai huỳnh quang tại chỗ: phát hiện các bất thường trong gen RUNX1, RUNX1T1, CBFB và MYH11.
Điều trị
Hóa trị dẫn đầu (induction chemotherapy)
Phương pháp điều trị truyền thống cho bệnh bạch cầu cấp dòng tủy với chuyển vị là hóa trị liệu dẫn đầu bằng thuốc tương tự nucleoside liều cao (cytarabine và fludarabine) với tỉ lệ thành công đạt 50–60% trường hợp. Theo dữ liệu từ nhóm nghiên cứu Ung thư và Bệnh bạch cầu tại Hoa Kỳ (Cancer and Leukemia Group B), trường hợp sử dụng 2 đến 4 chu kỳ thuốc cytarabine cho kết quả tốt hơn so với 1 chu kỳ.
Cấy ghép tế bào gốc (stem cell transplant)
Đối với các bệnh bạch cầu cấp dòng tủy khác, bệnh nhân thường thuyên giảm lần đầu sẽ được ghép tế bào gốc nhằm tăng cơ hội chữa khỏi bệnh. Tuy nhiên, người mắc bệnh bạch cầu cấp dòng tủy với chuyển vị thường được xem xét cấy ghép tế bào gốc trong lần thuyên giảm thứ hai do phương pháp hóa trị sử dụng trong giai đoạn đầu cho hiệu quả điều trị tốt hơn.
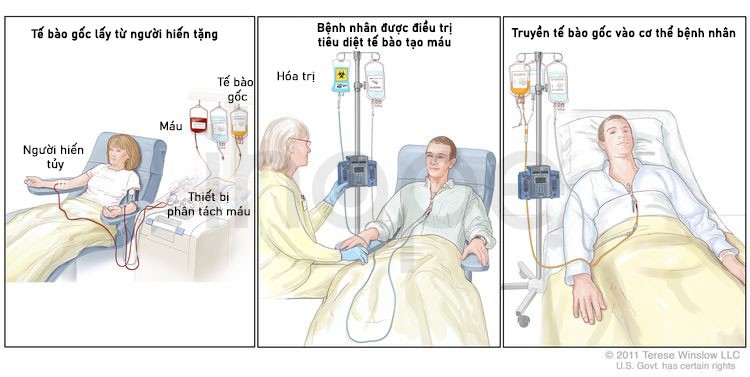
Nguồn: National Cancer Institute
Gemtuzumab ozogamicin
Kết hợp gemtuzumab ozogamicin (Mylotarg, Pfizer) vào phác đồ điều trị giúp cải thiện sức khỏe cho những bệnh nhân mắc bạch cầu cấp dòng tủy với chuyển vị. Theo dữ liệu từ MD Anderson cũng như Hội đồng Nghiên cứu Y khoa Vương quốc Anh, sử dụng kết hợp gemtuzumab ozogamicin có thể cải thiện kết quả so với chế độ điều trị truyền thống.
Dạng di truyền
Bạch cầu cấp dòng tủy với chuyển vị không di truyền mà phát sinh do các chuyển vị trên vật chất di truyền trong tế bào sau thụ tinh.
Phòng ngừa
Hiện nay chưa có các phòng ngừa bệnh bạch cầu cấp dòng tủy với chuyển vị.
Các tên gọi khác
- CBF acute myeloid leukemia
- CBF-AML
- Core-binding factor AML
References
- Genetic Testing Information. Acute myeloid leukemia. Retrieved December 21, 2023 from https://www.ncbi.nlm.nih.gov/gtr/conditions/C0023467/
- Catalog of Genes and Diseases from OMIM. LEUKEMIA, ACUTE MYELOID; AML. Retrieved December 21, 2023 from https://omim.org/entry/601626
- MedlinePlus. Core binding factor acute myeloid leukemia. Retrieved December 21, 2023 from https://medlineplus.gov/genetics/condition/core-binding-factor-acute-myeloid-leukemia/
- Millennium Medical. Evolving Strategies for the Management of Core-Binding Factor Acute Myeloid Leukemia Retrieved December 21, 2023 from https://www.hematologyandoncology.net/archives/november-2020/evolving-strategies-for-the-management-of-core-binding-factor-acute-myeloid-leukemia/
- Nature. Core binding factor acute myelogenous leukemia-2021 treatment algorithm. Retrieved December 21, 2023 from https://www.nature.com/articles/s41408-021-00503-6
- ScienceDirect. The core concepts of core binding factor acute myeloid leukemia: Current considerations for prognosis and treatment. Retrieved December 21, 2023 from https://www.sciencedirect.com/science/article/abs/pii/S0268960X23000784?viaihub
- ScienceDirect. Diagnosis and management of AML in adults: 2022 recommendations from an international expert panel on behalf of the ELN. Retrieved December 21, 2023 from https://www.sciencedirect.com/science/article/pii/S0006497122008874
- Spandidos Publications. Core binding factor acute myeloid leukemia: Advances in the heterogeneity of KIT, FLT3, and RAS mutations (Review). Retrieved December 21, 2023 from https://www.spandidos-publications.com/10.3892/mco.2020.2052#